EGFR肺癌靶向治療二十年來新突破! 臨床研究證實,靶向EGFRex20ins的新型靶向藥,治療緩解率達到43%(美中報道)
表皮生長因數受體(EGFR)突變是肺癌中最為常見的基因突變型之一,尤其在亞裔族群中,有40-60%的肺癌患者會攜帶EGFR突變。
自從1988年EGFR首次被發現可作為抗腫瘤藥物靶點,針對常見EGFR突變的靶向抑制劑已陸續更新了三代。然而針對比較少見的突變型,如僅占EGFR突變4-12%的第20號外顯子插入突變(EGFRex20ins),二十多年來始終沒有療效較好的靶向藥物被發現。
近日,來自Memorial Sloan Kettering癌症中心的Gregory J.Riely團隊,在Cancer Discovery上報道了一種可有效靶向EGFRex20ins突變的口服藥物mobocertinib(TAK-788;AP32788),及其在非小細胞肺癌(NSCLC)患者中的臨床I/II期臨床數據。
研究發現,mobocertinib在NSCLC中對多種EGFRex20ins突變均有抗腫瘤活性,其回應率達到了43%。此外在臨床試驗階段,mobocertinib的安全性良好,副作用與現有的EGFR抑制劑也十分相似。
EGFR是一種位於細胞膜上的受體,管控著與細胞生長、增殖、分裂、及死亡相關的多條通路。而發生突變的EGFR蛋白會始終處於被啟動的狀態,從而成為了促進細胞異常增殖表達的致癌源頭。
由於野生型EGFR廣泛表達於表皮及粘膜組織,所以在設計EGFR靶向抑制劑時,需要區分出對突變型EGFR的選擇特異性,來避免抑制野生型EGFR導致的胃腸道及皮膚黏膜相關副作用。
EGFRex20ins突變之所以一直處於“無藥可治”的境地,就是因為這種突變導致的結構變化與常見突變不同,現有的EGFR抑制劑對此突變型及野生型EGFR並沒有很大的選擇性差異。
在2020年,武田制藥的mobocertinib得到了美國FDA的突破性療法認定,填補了EGFRex20ins突變在臨床治療上長久以來的空缺。
Mobocertinib是一款EGFR不可逆小分子抑制劑。在臨床前試驗中[2],研究人員測試了mobocertinib對5種EGFRex20ins突變株(FQEA,NPG,ASV,NPH,和SVD)的生長抑制活性,發現mobocertinib對5種突變株的活性比現有的所有EGFR抑制劑都強,半數抑制濃度(IC50)達到了4.3–22.5nM。
此外,mobocertinib還對其他多種EGFR突變具有廣譜活性,其中就包括了常見的T790M及L858R突變。
相似的結果在多種動物腫瘤模型試驗中也得到了重現。在臨床前抑瘤試驗中,mobocertinib對EGFRex20ins NPH突變腫瘤模型的抑瘤率達到了87%,顯著高於第三代EGFR抑制劑osimertinib。
如果說mobocertinib在臨床前階段顯示出來對EGFR突變型的高度特異性和廣譜性僅僅是點燃了一絲希望,那麼之後其在臨床試驗上的初期數據則足以讓所有人對mobocertinib的未來翹首以盼。
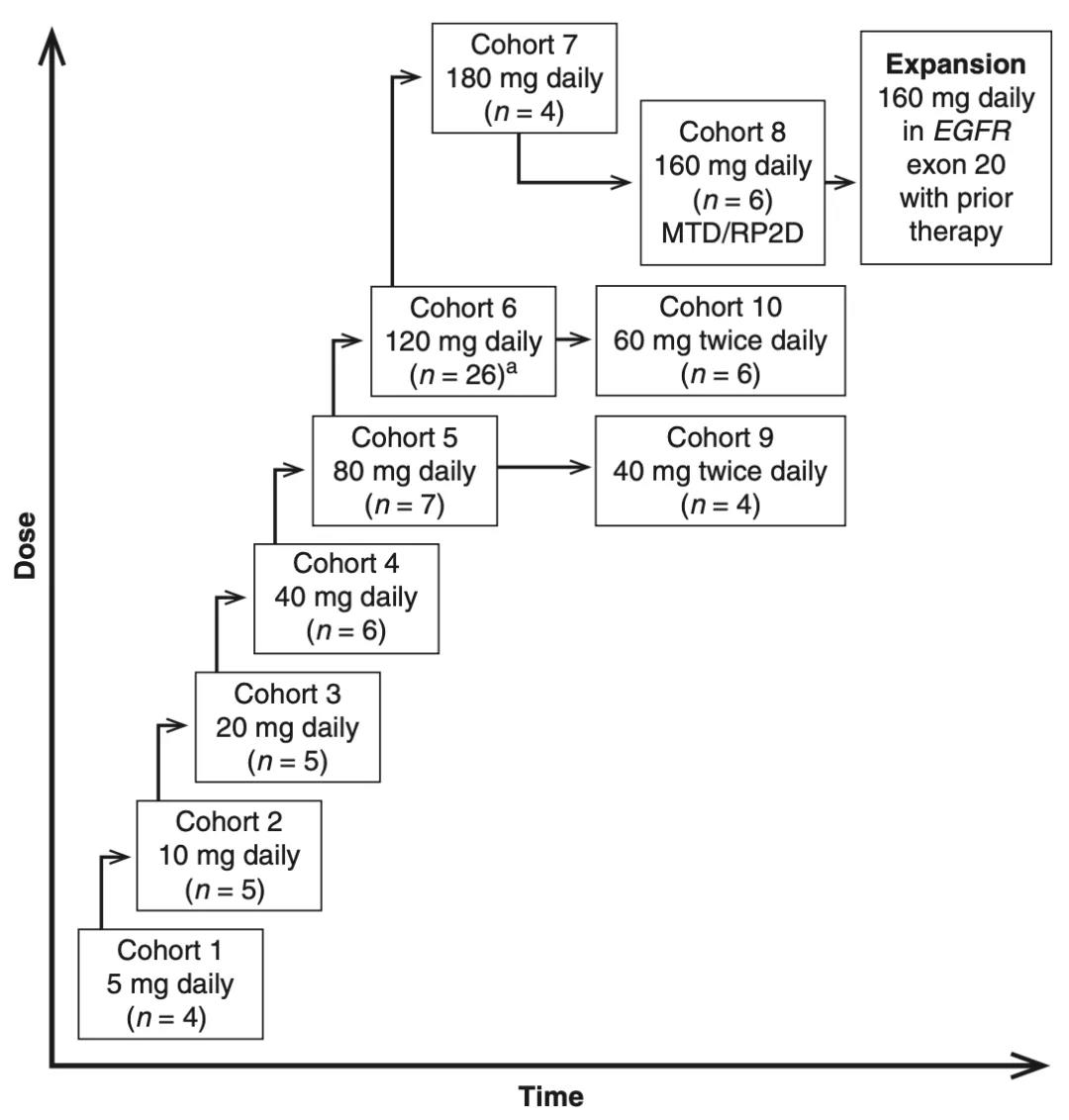
Mobocertinib的臨床I/II期試驗由Gregory J.Riely及其團隊發起,在美國28家醫院中開展。I期的劑量遞增試驗遵循傳統的3+3設計,共有73位對標準治療方案無效的IIIB/IV期NSCLC患者被納入此輪研究。
其中有44例可用於評價劑量限制毒性(DLT):20位每日口服5-40mg mobocertinib的患者中沒有毒性案例報導,7位每日口服120mg的患者中有一位發生了3級肺炎,7位每日口服120mg的患者中有一位發生了5級肺炎,6位每日口服160mg的患者中有一位發生了3級粘膜炎,而在4位每日口服180mg的患者中,有2位患者出現3級腹瀉。
因此研究人員將mobocertinib的最大耐受劑量定為160mg每日一次,並將其作為II期試驗的統一標準劑量。
截至2020年1月,試驗共納入136位NSCLC患者,其中70位患者攜帶EGFRex20ins突變,28位攜帶EGFRex20ins突變的患者接受了每日160mg的mobocertinib治療。
在這28位患者中,mobocertinib治療回應率達到43%(95%CI,24-63%),中位回應期為14個月,中位無進展生存期為7.3個月。患者攜帶的EGFRex20ins突變種類各異,但本試驗由於樣本量較少,並未發現對mobocertinib回應較突出的亞型。
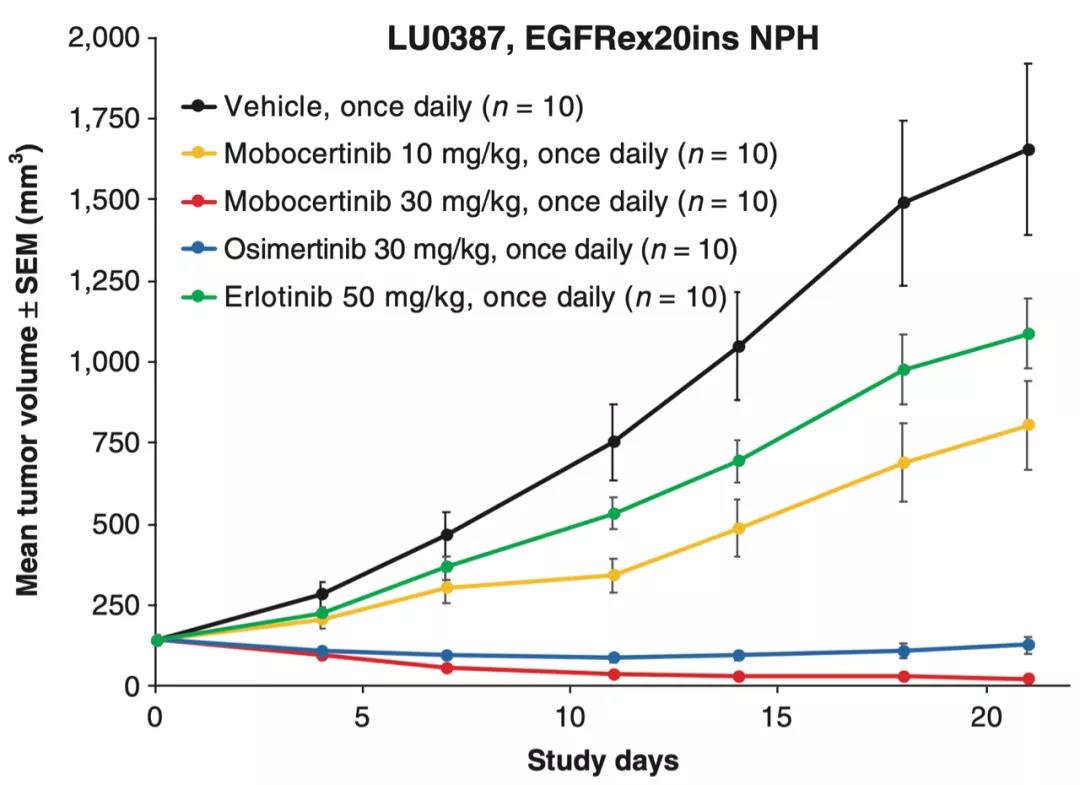 Mobocertinib,osimertinib及erlotinib对LU0387肿瘤模型的抑瘤曲线比较
Mobocertinib,osimertinib及erlotinib对LU0387肿瘤模型的抑瘤曲线比较
在對腫瘤腦轉移的臨床活性方面,mobocetinib在腦轉移組的客觀回應率為25%,中位無進展生存期為3.7個月;無腦轉移組客觀回應率56%,中位無進展生存期為10.2個月。說明mobocertinib對腦部轉移腫瘤的療效有限,而研究人員也因此在試驗後期不再納入處於腦轉移活性期的患者。
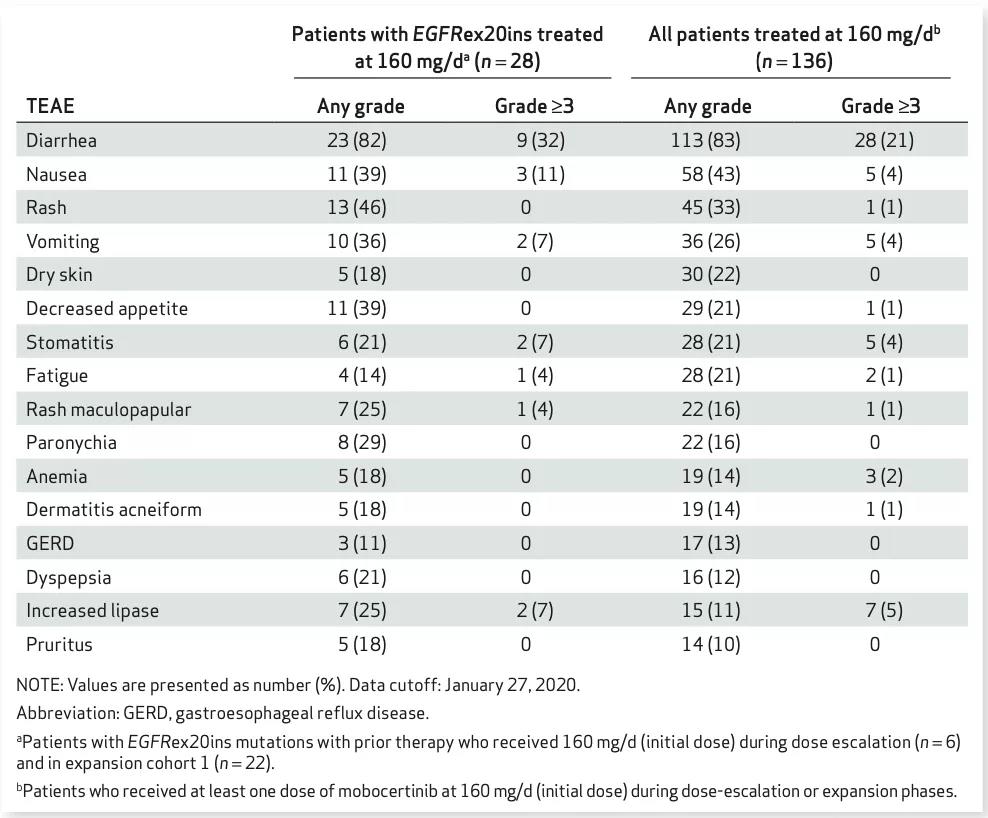
安全性方面,在所有納入試驗的136位患者中,134人(99%)發生了不良反應事件(TEAE),其中131人(96%)的TEAE被認為與mobocertinib相關,54位患者(40%)發生了3級及以上不良反應事件。在28位接受了每日160mg治療的EGFRex20ins突變患者中,有5位(18%)因副作用而降低了劑量,有7位(25%)因副作用導致停藥。
臨床試驗階段發現的最常見的治療相關不良事件為:腹瀉(83%)、噁心(43%)、皮疹(33%)和嘔吐(26%)。最為嚴重的不良反應是腹瀉,有21%的患者發生了三級及以上腹瀉,5%的患者因腹瀉而導致停藥。
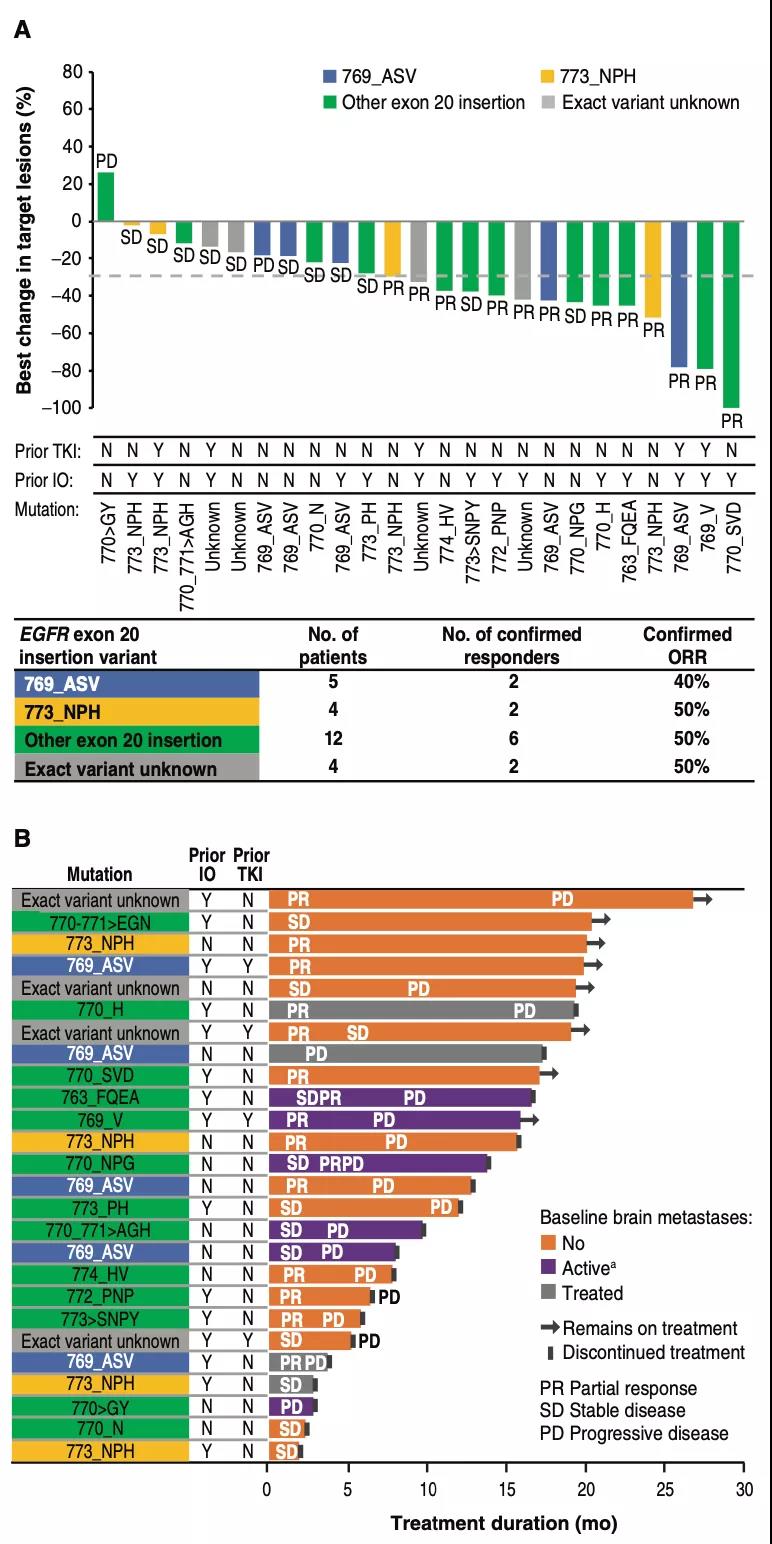 28位接受160mgdmobocertinib治疗的EGFRex20ins突变患者疗效示意图
28位接受160mgdmobocertinib治疗的EGFRex20ins突变患者疗效示意图
然而,正如上文所說,EGFR在胃腸道粘膜組織中廣泛表達,因此胃腸道副作用在EGFR抑制劑中普遍存在。早期的EGFR抑制劑厄洛替尼、吉非替尼、阿法替尼和達可替尼均存在18-95%不等的腹瀉率及高達25%的3級及以上腹瀉率[3],第三代EGFR抑制劑奧希替尼雖然3級及以上腹瀉率較低(0.3%),但是也存在47%左右的1-2級腹瀉率。
鑒於mobocertinib的腹瀉副作用依然較高,研究人員在試驗後期也及時調整了試驗方案,允許在患者出現一級腹瀉時即開始啟用腹瀉治療。
綜上所述,mobocertinib在臨床上的療效可圈可點,安全性良好。
正是基於本試驗的數據,mobocertinib於2020年4月獲得FDA的突破性治療認證,用於攜帶EGFRex20ins突變晚期NSCLC患者鉑類化療或一線治療進展後的二線治療。
雖然本試驗的樣本量較少,但是試驗中mobocertinib對EGFRex20ins突變NSCLC的回應率達到了43%,相較於使用一二代EGFR抑制劑治療EGFRex20ins突變的客觀回應率8-27%,以及使用多西他賽化療的回應率14%,mobocertinib在今後大規模III期試驗的表現著實令人期待。
在II期擴展試驗中研究人員也單獨設置了monocertinib用於EGFRex20ins突變晚期NSCLC患者一線治療的試驗組,期待不久的將來能看到monocertinib用於一線治療的臨床數據問世!(原創 奇點糕)